

13/10/2022
Tóm tắt
Đánh giá tính an toàn chế phẩm sinh học, mức độ độc hại ở mức độ di truyền, ảnh hưởng đến quần thể đa dạng sinh học là hết sức cần thiết với đơn vị khảo nghiệm và cơ quan quản lý. Nhóm nghiên cứu đã lựa chọn 6 chế phẩm đại diện đánh giá độc tính bán trường diễn trên phôi cá ngựa vằn để đánh giá tỷ lệ nở, gây chết, quái thai. Kết quả thí nghiệm cho thấy, 3 mẫu M1 (enzym Blend), M4 (TRACATU), M5 (Remediator (Việt Nam)) an toàn; M2 (Prozym), M3 (Tictac), M6 (Remediator (Enretech, Australia)) có độc tính thấp nhưng vẫn thuộc nhóm an toàn. Các phương pháp thể hiện sự phù hợp và kết quả tin cậy trong quá trình thực hiện.
Từ khóa: An toàn chế phẩm sinh học; độc tính bán trường diễn.
Nhận bài: Ngày 19/9/2022; Sửa chữa: Ngày 21/9/2022; Duyệt đăng: Ngày 23/9/2022.
1. Mở đầu
Tại Điều 6, Luật Bảo vệ môi trường năm 2020 quy định: Cấm phát tán, thải ra môi trường các chất độc hại đến sức khỏe con người, sinh vật và tự nhiên. Hiện nay đã có nhiều phương pháp trong nước và quốc tế hướng dẫn đánh giá độc tính của các chất. Do vậy, xác định phương pháp hiện đại có độ tin cậy cao và phù hợp với điều kiện cơ sở vật chất Việt Nam là rất cần thiết.
Việc sử dụng cá và động vật trong nhiều thí nghiệm đánh giá độc tính trên thế giới đang bị hạn chế do Luật Bảo vệ động vật. Vì vậy, thay bằng việc sử dụng cá trong thí nghiệm về độc tính, ngày nay nhiều thử nghiệm bắt đầu sử dụng phôi cá. Ngoài ứng dụng để xác định độc tính cấp tính, phôi cá còn là mô hình phù hợp cho các nghiên cứu nhằm tìm hiểu các cơ chế gây độc và xác định các tác động có hại mang tính tích lũy lâu dài có thể xảy ra cho cá thể và quần thể (Wang et al., 2020). Nhóm nghiên cứu đã lựa chọn 6 chế phẩm sinh học đại diện cho các dạng chế phẩm có nguồn gốc trong nước và quốc tế đang được lưu hành trên thị trường để đánh giá độc tính bán trường diễn trên đối tượng là phôi cá ngựa vằn.
2. Thí nghiệm và phương pháp nghiên cứu
2.1. Mẫu thí nghiệm
6 mẫu thí nghiệm:
(1) M1: mẫu enzym Blend xử lý nước (Nhập khẩu từ Mỹ)
Thành phần trong 1kg: Protease: 5.200.000 U; Amylase: 1.560.000 U; Cellulose: 1.300.000 U;Xylanase: 1.300.000 U; Tá dược vừa đủ 1 kg
(2) M2: Prozym
Thành phần trong 1kg: Protease: 3500 UI/ml; Lipase: 1500 UI/ml; Amylase: 2000 UI/ml; Cellulase: 1500 UI/ml; hemicellulase: 1200 UI/ml; Tá dược vừa đủ 1 kg
(3) M3: men bể phốt Tictac
Thành phần gồm các loại vi sinh vật hữu ích, phân giải các chất thải như xenluloza, protein, tinh bột.
(4) M4: micro Phốt TRACATU
Thành phần gồm hàng tỉ vi sinh vật hiếu khí và yếm khí. Nồng độ 65g bột/500 ml dịch thể
(5) M5: Remediator (Việt Nam)
M5 là chất rất thô, bao gồm rất nhiều thành phần mang hình dạng khác nhau: hạt, sợi, tấm… Dung dịch pha từ M5 có phần lắng cặn, phần nổi và khuếch tán tan đều trong dung dịch E3.
(6) M6: Remediator (Enretech, Australia)
M6 là chất bột thô, màu trắng ngà, tan không hoàn toàn trong dung môi E3. Dung dịch E3 lắng rất nhanh xuống đáy ống, trước khi thử nghiệm cần lắc kỹ trước khi thử nghiệm.
2.2. Vật liệu và phương pháp nghiên cứu
2.2.1. Vật liệu nghiên cứu
- Bể nuôi cá,
- Đĩa nhựa 6 giếng,
- Kính hiển vi,
- Pipet đầu tip,
- Máy đo pH,
- Máy đo nồng độ oxy,
- Máy đo độ cứng của nước,
- Tủ ấm có thể điều chỉnh nhiệt độ đến 26 +-1oC
- Các ống thủy tinh và bình thủy tinh để pha mẫu.
- Dung dịch E3 (dung dịch nuôi phôi, chứa 5 mM NaCl 0.17 mM KCl, 0.33 mM CaCl2, 0.33 mM MgSO4).
Thử nghiệm độc tính được thực hiện trên đối tượng phôi cá ngựa vằn (Daniorerio) theo hướng dẫn thử độc cấp tính của hóa chất trên phôi cá của OECD (OECD guideline 236) [OECD, Test No. 236], với quy trình thực hiện được như sau:
Chuẩn bị nước và điều kiện thử nghiệm: Nước sử dụng cho thí nghiệm nên đạt độ cứng được khuyến cáo khoảng 100-300 mg/L CaCO3. Độ pH của nước nằm trong khoảng từ 6.5-8.
Chuẩn bị phôi cá: Phôi cá trong giai đoạn từ 2-8 tế bào (khoảng 1-2 giờ sau khi thụ tinh).
Chuẩn bị mẫu thử nghiệm: Các mẫu dạng bột sẽ được pha ra nồng độ dung dịch gốc 5000 mg/L. Dải nồng độ sử dụng dựa trên tham chiếu của GHS về nồng độ LC50 trên thử nghiệm độc tính cấp (Bảng 1), nồng độ sử dụng trong thí nghiệm là: 500 - 1000 - 2000 - 3000 - 5000 mg/L đều được pha trong dung dịch E3 (dung dịch nuôi phôi, chứa 5 mM NaCl 0.17 mM KCl, 0,33 mM CaCl2, 0,33 mM MgSO4). Riêng M4 là mẫu ở dạng lỏng và không rõ nồng độ, chúng tôi thử nghiệm bằng cách pha loãng hóa chất trong theo tỷ lệ 1:2 và 1:4 trong dung dịch E3.
Thiết kế thử nghiệm: Đĩa thử nghiệm độc tính là đĩa 6 giếng (SPL), mỗi giếng được bổ sung 4ml dung dịch. Giếng đối chứng chứa dung dịch E3, 5 giếng còn lại chứa các dung dịch theo 5 nồng độ đã chuẩn bị. Mật độ phơi nhiễm là 20 cá thể/giếng. Mỗi 24h, số lượng phôi chết và dị dạng được ghi chép lại cho đến thời điểm 96h, thử nghiệm được lặp lại 3lần.
Phân tích số liệu và tiêu chí đánh giá
Kết quả thu thập từ các lần lặp lại được sử dụng để xây dựng đường cong đáp ứng liều và tính toán giá trị LC50 (Lethal Concentration 50 - nồng độ gây tử vong 50% cá thể thí nghiệm), EC50 (Effective Concentration 50–nồng độ gây ảnh hưởng hình thái lên 50% cá thể thí nghiệm) và TI (Tetratogenic index – chỉ số gây quái thai, được tính bằng tỷ lệ LC50/EC50) trên phần mềm GraphPad Prism8.0. Chỉ số LC50 sẽ được so sánh với tiêu chuẩn thử nghiệm độc tính cấp của GHS để phân loại độc tính (Vereinte Nationen, 2021). Chỉ số TI cùng với EC50 được sử dụng để dự đoán khả năng xuất hiện bất thường hình thái trong trường hợp chất không gây tử vong phôi, TI >= 3 và EC50 < 1.000 μM cho thấy chất có tiềm năng cao gây quái thai trên phôi (Jarque et al., 2020).
Bảng 1: Đánh giá LC50 (Acute toxicity estimate - ATE) theo tiêu chuẩn GHS
|
Đường tiếp xúc |
Độc độ 1 |
Độc độ 2 |
Độc độ 3 |
Độc độ 4 |
Độc độ 5 |
|
Ăn/Uống (mg/kg P)
|
ATE≤5 |
5˂ATE≤ 50 |
50˂ATE≤300 |
300˂ATE≤2000 |
2000˂ATE≤5000 |
|
Da (mg/kg P)
|
ATE ≤ 50 |
50˂ATE≤200 |
200˂ATE≤1000 |
1000˂ATE≤2000 |
|
|
Không khí (ppmV) |
ATE≤100 |
100˂ATE≤500 |
500˂ATE≤2500 |
2500˂ATE≤20000 |
|
|
Hơi (mg/L) |
ATE≤0.5 |
0.5˂ ATE≤ 2.0 |
2.0˂ATE≤10.0 |
10.0˂ATE≤20.0 |
|
|
Bụi và sương mù (mg/L)
|
ATE≤0.05 |
0.05˂ATE≤0.5 |
0.5˂ATE≤1.0 |
1.0˂ATE≤ 5.0 |
|
3. Kết quả và thảo luận
Kết quả thí nghiệm thu được sẽ được trình bày theo lần lượt từng mẫu thí nghiệm từ M1 - M6.
3.1. Kết quả thử nghiệm mẫu M1
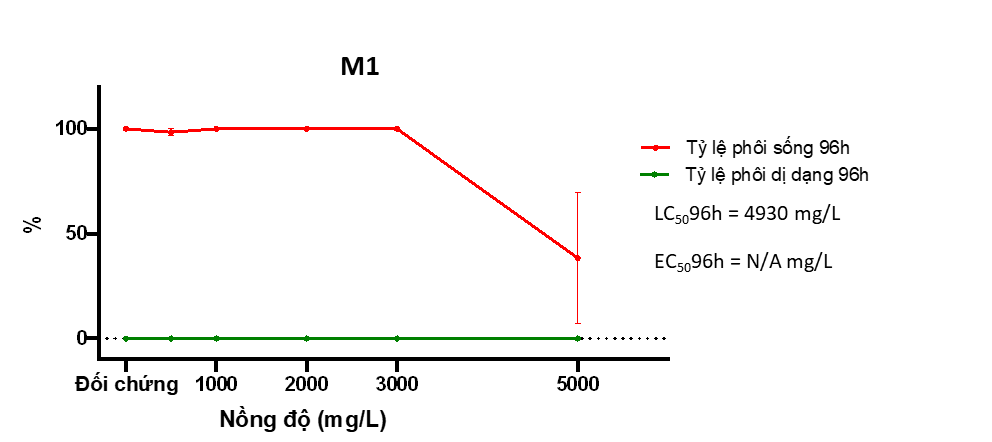
Hình 1. Đồ thị tỷ lệ sống và dị dạng của phôi cá khi thử nghiệm với M1
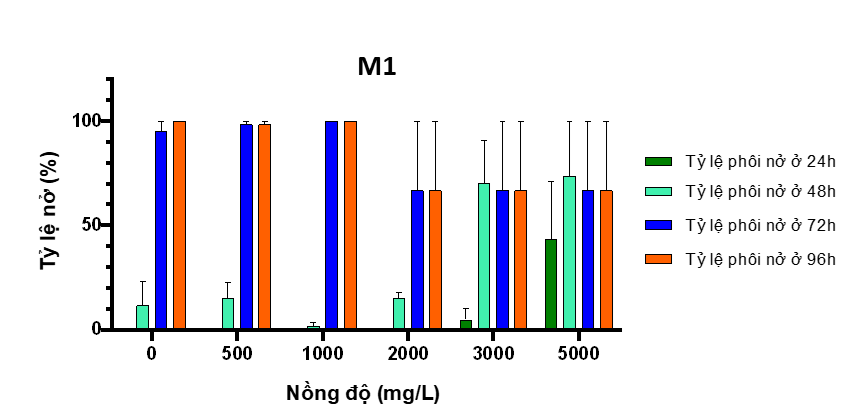
Hình 2. Đồ thị tỷ lệ nở của phôi cá khi phơi nhiễm với M1
Kết quả trên cho thấy:
+ M1 không gây ảnh hưởng lớn lên sức sống của phôi, chỉ ở nồng độ 5.000 mg/L mới xuất hiện phôi tử vong ở tỷ lệ = 61.6 %. Giá trị LC50 tính toán được là 4.930 mg/L, năm trong khoảng 2.000 – 5.000 mg/L (Hình 1), như vậy M1 thuộc nhóm 5 – nhóm rất an toàn theo thang phân loại GHS.
+ Các phôi sống cũng không xuất hiện bất thường trên hình thái sau 96h phơi nhiễm, không tính toán được giá trị EC50.
+ Đáng chú ý, M1 có thể gây nở sớm ngay từ 24h ở nồng độ 3.000 - 5.000 mg/L, đặc biệt ở nồng độ 5.000 mg/L (Hình 2).
+ Hiện tượng phôi nở sớm của M1 được thể hiện trong Hình 2 và 3. Ở nồng độ 5.000 mg/L, các phôi đã phá vỡ vỏ ngay từ 24h. Ngoại trừ hiện tượng nở sớm, hình thái và giai đoạn phát triển của lô thí nghiệm không có biểu hiện bất thường.
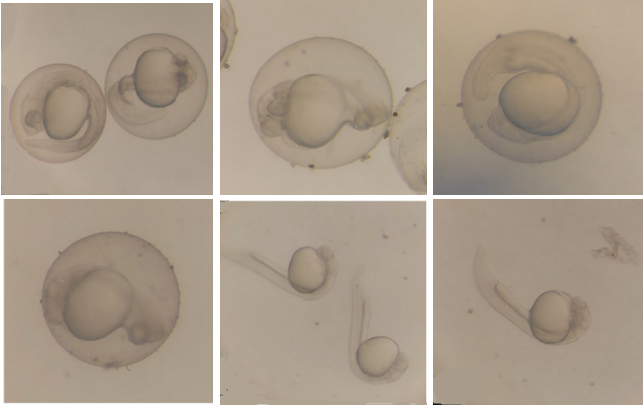
Hình 3. Hình ảnh chụp phôi thử nghiệm với M1 tại thời điểm 24h ở độ phóng đại 50X

Hình 4. Hình ảnh chụp phôi thử nghiệm với M1 tại thời điểm 24h ở độ phóng đại 10X
3.2. Kết quả thử nghiệm mẫu M2
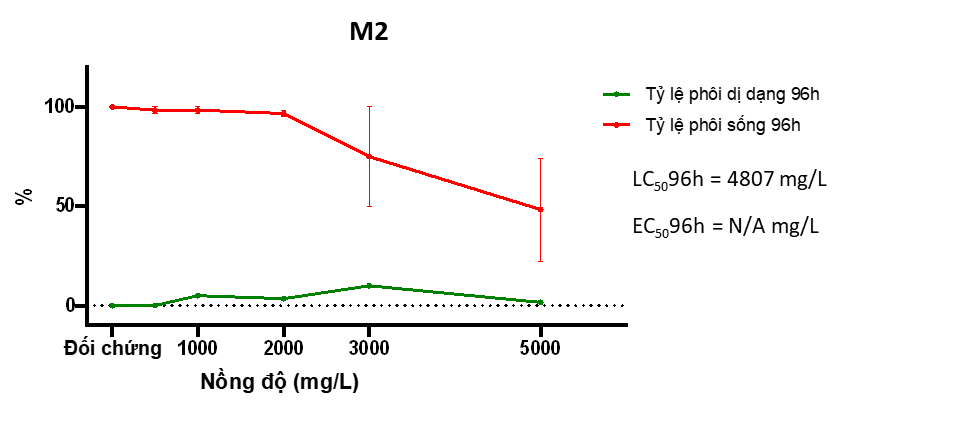
Hình 5. Đồ thị tỷ lệ sống và dị dạng của phôi cá khi thử nghiệm M2
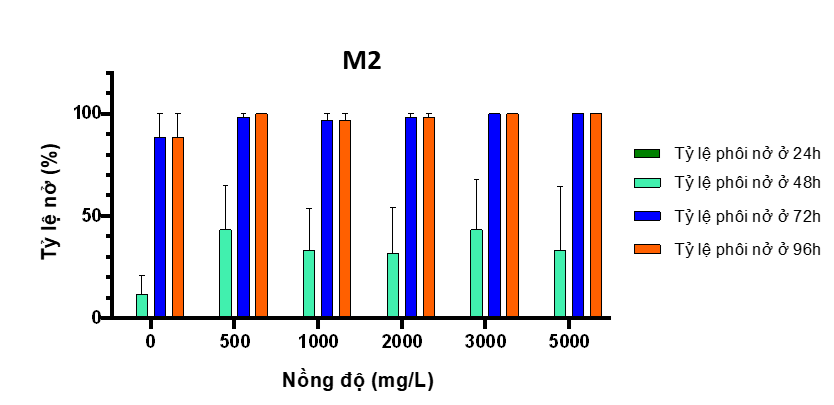
Hình 6: Đồ thị tỷ lệ sống và dị dạng của phôi cá khi thử nghiệm với M2
Kết quả trên cho thấy:
+ M2 gây ảnh hưởng đến sức sống của phôi từ nồng độ 3.000 mg/L, độc tính của M2 tăng theo chiều tăng của nồng độ nhưng ở 5000 mg/L tỷ lệ tử vong của phôi mới chỉ đạt tới xấp xỉ 51%. Dị dạng trên phôi xuất hiện ở tỷ lệ thấp ở 2.000 – 5.000 mg/L dưới 20%. Không tính toán được chỉ số EC50 (Hình 5).
+ M2 không gây ảnh hưởng đến khả năng nở của phôi, các phôi đều nở vào thời điểm tương đương với đối chứng (Hình 6).
3.3. Kết quả thử nghiệm mẫu M3
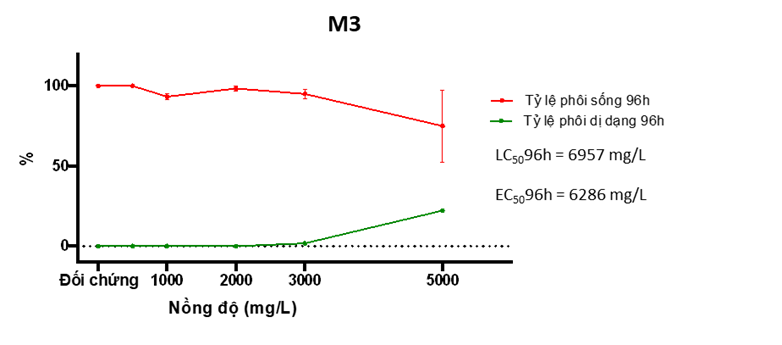
Hình 7. Đồ thị tỷ lệ sống và dị dạng của phôi cá khi thử nghiệm M3
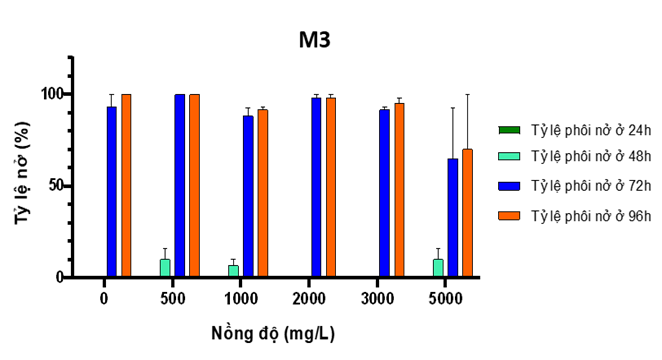
Hình 8: Đồ thị tỷ lệ nở của phôi cá khi phơi nhiễm với M3
Kết quả trên cho thấy:
+ M3 gây tử vong thấp ở các nồng độ, tỷ lệ đạt cao nhất tại nồng độ 5.000 mg/L ở mức 25%. LC50 ở 96h tính toán được ở mức 6.957 mg/L > 5.000 mg/L (Hình 7) cho thấy M3 có tính độc rất thấp, thuộc nhóm chất không độc (mức 5) theo thang đánh giá của GHS [2].
+ M3 có ảnh hưởng đến hình thái phôi ở nồng độ 5.000 mg/L, dị dạng quan sát được là phù màng tim (Hình 9), tuy nhiên do số lượng phôi bị ảnh hưởng rất thấp, hệ số EC50 tính toán được ở mức rất cao 6.286 mg/L, cho thấy khả năng chất gây dị dạng rất yếu.
+ Tỷ lệ nở khi phơi nhiễm với M3 chỉ bất thường ở nồng độ 5.000 mg/L do phôi đã tử vong trước khi nở (Hình 8)




Hình 9. Phôi cá khi phơi nhiễm với M3; Đầu mũi tên chỉ vị trí phù màng tim
3.4. Kết quả thử nghiệm với mẫu M4
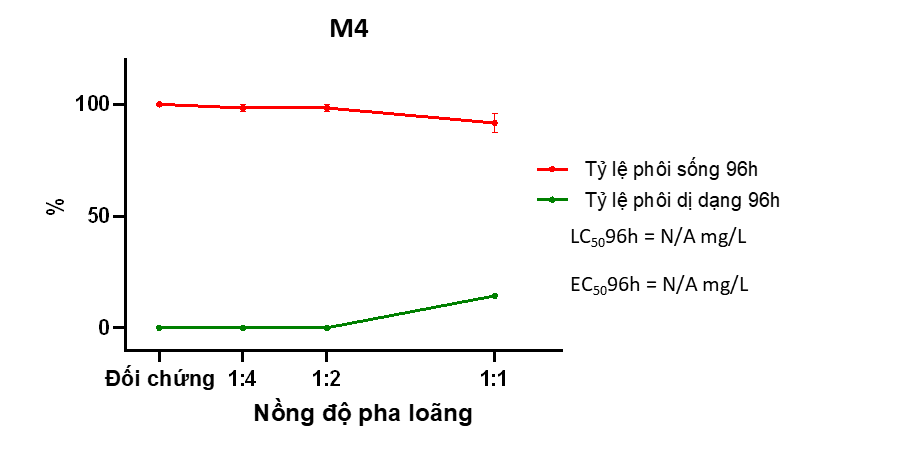
Hình 10. Đồ thị tỷ lệ phôi sống và dị dạng của phôi cá khi thử nghiệm với M4. Tỉ lệ pha loãng 1:1 tương đương với nồng độ 65000mg/L, tỉ lệ pha loãng 1:2 tương đương với nồng độ 37500 mg/L, tỉ lệ pha loãng 1:4 tương đương với nồng độ 18250 mg/L
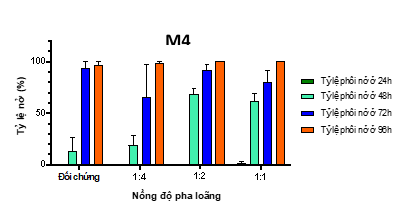
Hình 11. Đồ thị tỷ lệ nở tại của phôi cá khi phơi nhiễm với M4; Tỉ lệ pha loãng 1:1 tương đương với nồng độ 65.000mg/L, tỉ lệ pha loãng 1:2 tương đương với nồng độ 37.500 mg/L, tỉ lệ pha loãng 1:4 tương đương với nồng độ 18.250 mg/L
Kết quả trên cho thấy:
+ M4 ảnh hưởng rất ít đến sức sống của phôi cá ngựa vằn, chỉ quan sát được dị dạng phù màng tim ở mức 17% tại nồng độ nguyên chất 1:1 (tương đương với nồng độ 65.000mg bột/L) (Hình 10).
+ Do đó giá trị LC50 và EC50 không tính toán được. M4 cũng không gây ảnh hưởng đến tỷ lệ nở của phôi sau 96h phơi nhiễm (Hình 11).
3.5. Kết qủa thử nghiệm với mẫu M5
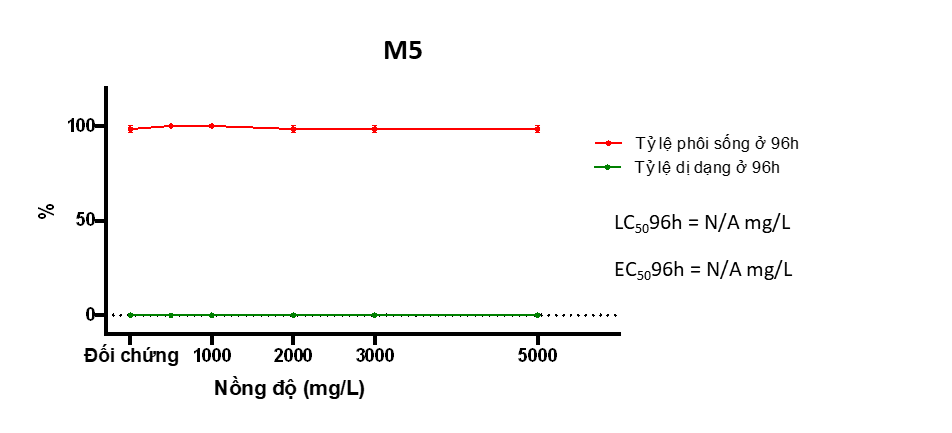
Hình 12. Đồ thị tỷ lệ sống, dị dạng và tỷ lệ phôi nở khi phơi nhiễm với M5
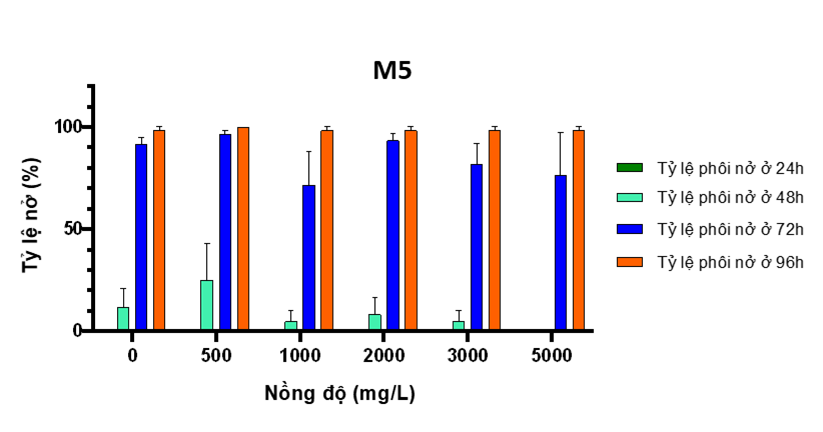
Hình 13. Đồ thị tỷ tỷ lệ phôi nở khi phơi nhiễm với M5
Kết quả trên cho thấy:
+ M5 không gây ảnh hưởng lên phát triển phôi cá ở cả 3 tiêu chí: tử vong, dị dạng và nở.
+ Các chỉ số của phôi thí nghiệm tương đương với đối chứng (Hình 2.12, 2.13) do đó không xác định được các chỉ số LC50 và EC50
3.6. Kết quả thử nghiệm độc tính mẫu M6
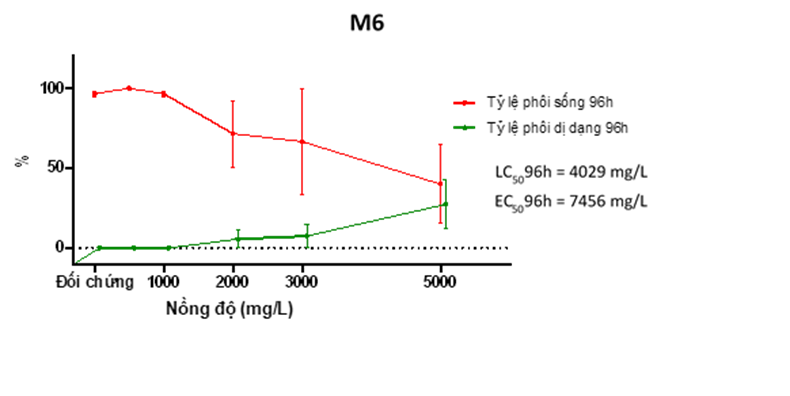
Hình 14. Đồ thị tỷ lệ sống và dị dạng của phôi cá khi thử nghiệm với M6
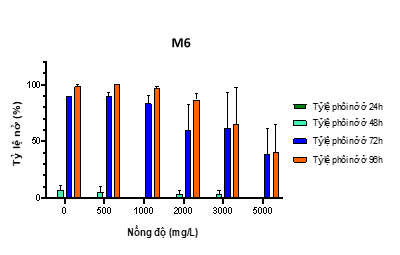
Hình 15. Đồ thị tỷ lệ phôi nở tại 4 thời điểm khi phơi nhiễm với M6
Kết quả trên cho thấy:
+ M6 có ảnh hưởng đến sức sống và hình thái của phôi cá ngựa vằn sau 96 giờ phơi nhiễm. Độc tính gây chết tăng dần theo nồng độ từ 1.000 – 5.000 mg/L, tỷ lệ cao nhất đạt 60% ở 5.000 mg/L (hình 14).
+ M6 chỉ có tác động mạnh lên khả năng nở của phôi ở các nồng độ cao: 3.000 và 5.000 mg/L tại thời điểm 96h (hình 15).
+ Tương tự, bất thường hình thái của phôi quan sát được từ nồng độ 2.000 mg/L và tỷ lệ dị dạng tăng dần theo nồng độ cho tới 5.000 mg/L. Phù màng bao tim là dị dạng duy nhất quan sát được khi phơi nhiễm M6 (Hình 16).
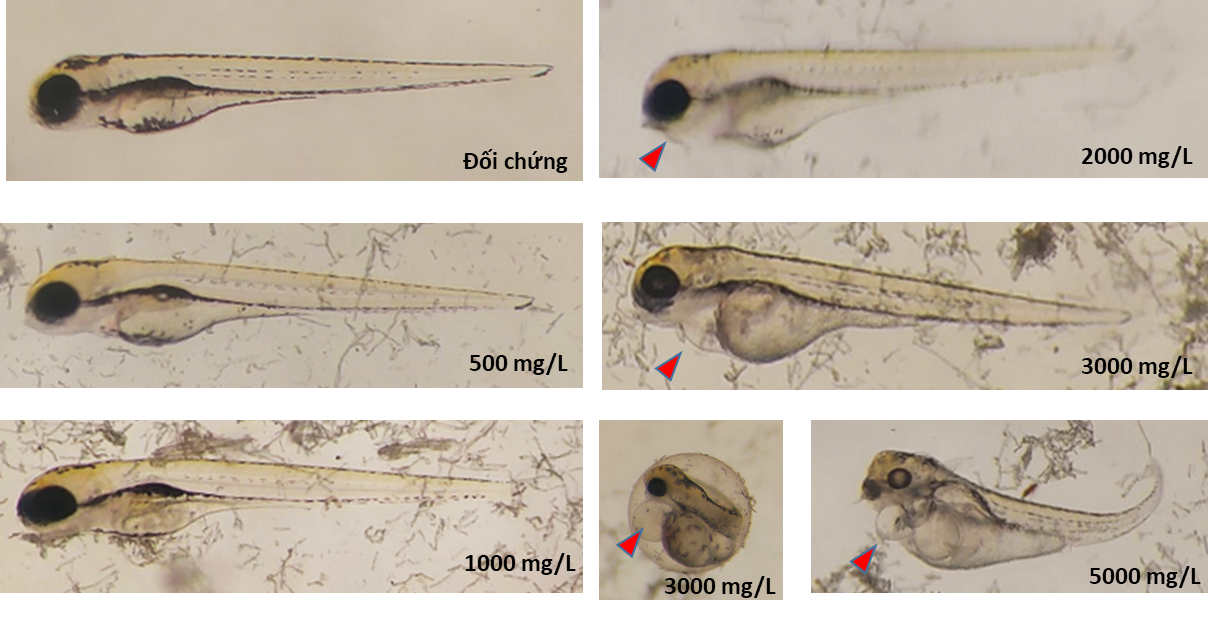
Hình 16. Hình ảnh phôi cá ngựa vằn khi phơi nhiễm với M6 ở 96 giờ. Mũi tên màu đỏ chỉ vị trí phù màng tim
4. Kết luận
- Về cơ bản, thử nghiệm trên phôi cá ngựa vằn đã đánh giá được độc tính của mẫu thử ngay từ giai đoạn sớm. Ngoài đánh giá về độc tính của mẫu thử, thử nghiệm này còn xác định được tác động của mẫu thử đến sự phát triển của phôi cũng như dị dạng dưới tác động của mẫu thử. Thử nghiệm này về cơ bản đã sẵn sàng để sử dụng như một sự thay thế đầy đủ cho các thử nghiệm cấp tính trên cá. Bên cạnh đó, 85% hệ gen tương đồng với hệ gen người và quá trình phát triển phôi tương tự như ở động vật bậc cao (Howe et al., 2013) là những yếu tố quan trọng đề thử nghiệm trên phôi cá ngựa vằn được áp dụng trong thử nghiệm đánh giá độ độc cấp tính.
- Kết quả đánh giá độc tính của của các mẫu M1-M6 được tổng hợp trong bảng 2. Theo đó, hệ số TI được tính bằng tỷ lệ LC50/EC50, nó cho phép đánh giá khả năng phôi mang dị dạng nếu còn sống khi tiếp xúc với hóa chất. TI >=3 cho thấy hóa chất có thể gây bất thường. Tất cả các mẫu thử nghiệm đều có TI < 3, do đó chúng đều không có khả năng gây quái thai.
Tài liệu tham khảo:
1. Belanger SE, Balon EK, Rawlings JM (2010) Saltatory ontogeny of fishes and sensitive early life stages for ecotoxicology tests. Aquat
Toxicol 97:88-95.
2. Braunbeck, Thomas; Kais, Britta; Lammer, Eva; Otte, Jens; Schneider, Katharina; Stengel, Daniel; Strecker, Ruben (2015). The fish embryo test (FET): origin, applications, and future. Environmental Science and Pollution Research, 22(21), 16247-16261.
3. Embry MR, Belanger SE, Braunbeck T, Galay-Burgos M, Halder M, Hinton DE, Léonard MA, Lillicrap A, Norberg-King T, Whale G
(2010). The fish embryo toxicity test as an animal alternative method in hazard and risk assessment and scientific research. Aquat Toxicol
97:79-87.
4. Howe K., Clark M.D., Toroja C.F., Torrance J., Berthelot C., Muffato M., Collins J.E., et al. "The zebrafish reference genome sequence and its relationship to the human genome”, Nature, 496 (2013) 498.
5. https://www.oecd-ilibrary.org/environment/test-no-202-daphnia-sp-acute-immobilisation-test_9789264069947-en.
6. Wang, Danting; Zhang, Yuhuan; Li, Jieyi; Dahlgren, Randy A.; Wang, Xuedong; Huang, Haishan; Wang, Huili (2020). Risk assessment of cardiotoxicity to zebrafish (Danio rerio) by environmental exposure to triclosan and its derivatives. Environmental Pollution, 265(), 114995-. doi:10.1016/j.envpol.2020.114995 .
7. Warne MS, VanDam R. 2008. NOEC and LOEC data should no longer be generate or used. Australas J Ecotox 14(4):1-5.
Phạm Thị Kiều Oanh1, Đỗ Thị Thảo2, Huỳnh Thị Thu Huệ3, Nguyễn Thị Thiên Phương1,Trần Quốc Trọng1*
(1) Vụ Khoa học, Công nghệ và Hợp tác quốc tế - Tổng cục Môi trường, Bộ Tài nguyên và Môi trường
(2) Viện Công nghệ sinh học, Viện Hàn lâm Khoa học và Công nghệ Việt Nam
(3) Viện nghiên cứu hệ gen, Viện Hàn lâm Khoa học và Công nghệ Việt Nam
(Nguồn: Bài đăng trên Tạp chí Môi trường, số Chuyên đề Tiếng việt III/2022)
Assessing acute and semi-chronic toxicities of severial bioproducts used for environmental protection in Vietnam
Phạm Thị Kiều Oanh1, Đỗ Thị Thảo2, Huỳnh Thị Thu Huệ3, Nguyễn Thị Thiên Phương1, Trần Quốc Trọng1*
(1) Department of Science, Technology and International Cooperation - Vietnam Environment Administration
(2) Institute of Biotechnology - Vietnam Academy of Science and Technology
(3) Institute of Genome Research - Vietnam Academy of Science and Technology
Abtract
Safety evaluation of bioproducts, levels of genetic toxicity, and the impact on biodiversity are essential for the testing units and the management agencies. The research team selected 06 representative samples for evaluating semi-chronic toxicity on zebrafish embryos with hatching, lethality, and teratogenic rates. Experimental results showed that 03 samples M1 (enzyme Blend wastewater treatment), M4 (micro Phốt, TRACATU), M5 (Remediator (Vietnam)) were safe; M2(Prozym), M3(Tictac), M6 (Remediator (Enretech, Australia)) had low toxicity at the permitted level. The method of the OECD guideline 236 on toxic testing demonstrated appropriation and reliability during the research.
Key word: Safety of bioproducts, semi-chronic toxicity.